盡管新的一次性技術提供了克服 ATMP 生產中的若干挑戰所需的靈活性,但生產商在進行規模放大時必須注意許多考慮因素和障礙。
自生物藥問世以來,其需求一直在增長,2020 年生物藥市場價值約為 3,026.3 億美元,預計到 2026 年將達到 5,092.3 億美元,復合年增長率為 9.06%。隨著研究和技術的進步,可用的生物藥種類日益繁多,包括單克隆抗體 (mAb)、預防性疫苗、基因治療病毒載體(主要是慢病毒和腺相關病毒)、細胞療法(例如嵌合抗原受體 T-細胞療法和改良干細胞)和溶瘤病毒(例如腺病毒、皰疹病毒和牛痘病毒)。
因此,生物反應器供應商和合同開發及制造組織(CDMO)行業面臨著擴大生產規模的壓力。為了滿足需求,這些行業必須切實擴大規模,同時考慮安全性、人工操作員處理、工程、基礎設施、成本,最后是生物工藝本身。
隨著對產能需求的增加,一次性技術 (SUT) 與上游和下游生產業務的整合也在增加,以用于臨床開發和商業供應。可用的 SUT 包括生物反應器、培養基和緩沖液制備、過程中混合和液體儲存等。它們越來越多的采用主要是由 SUT 提供的許多優勢推動的:
增加生產和運營
降低早期資本投資的靈活性(模塊化設計)
減少總占地
縮短運行周轉時間
降低運營成本
最大限度地減少交叉污染風險
實現簡單的安裝
提供有利于封閉工藝操作的設計
避免昂貴、費力且耗時的在線清洗/滅菌驗證(后者在生產病毒時尤其具有挑戰性)。
2018 年,超過 66% 的制藥公司被發現更喜歡 SUT 而不是“永久性”技術。
用于先進治療藥物產品的 SUT
隨著個性化醫療、孤兒藥和基因治療方式(通常被稱為先進治療藥物 [ATMP])的發展,SUT 可能會越來越受歡迎。
目前有超過 1,000 種 ATMP 正在臨床試驗當中,且可能最終實現商業化供應。典型的重磅炸彈 mAb 藥物需要非常大的生產規模,主要使用基于中國倉鼠卵巢 (CHO) 的平臺工藝和不銹鋼生物反應器,而 ATMP 通常需要 SUT 提供的生產和規模靈活性。
以前,不銹鋼生物反應器與一次性 (SU) 生物反應器相比具有特殊優勢:容量大,通常達到 10,000 - 20,000 L。大多數一次性生物反應器供應商將其產品限制在 2,000-2,500 L 規模。這部分是由于液體培養基重量增加和處理問題帶來的壓力挑戰。
然而,在過去五年中,一次性生物反應器已經成功商業化,工作體積可達 5,000 L(ThermoFisher、HyPerforma DynaDrive) 甚至 6,000 L(ABEC Inc.)。
在需要放大至超過單個一次性生物反應器所能提供的體積的情況下,必須考慮規模擴展(增加并行生物反應器的數量)或工藝強化(通常是高細胞密度灌流工藝)。然而,并不是所有的細胞系和工藝都容易馴化或適應灌流,從而帶來了額外的挑戰。
確定工藝可放大性
了解和確認 ATMP 在不同規模(包括商業化規模)的生產工藝是一項關鍵的監管要求,可保障產品質量和患者安全。因此,適當的工藝開發、表征、放大和驗證是重要的練習。
在考慮生產工藝(尤其是上游)的可放大性時,必須考慮許多重要因素。考慮這些方面是整個產品生命周期的重要組成部分,包括:
工程系統的固有可放大性(例如,生物反應器設計和關鍵工程參數)
生產工藝步驟
有機體的特性和特征(例如,哺乳動物細胞系,如 CHO 或 HEK293)
產生的產品(例如,mAb 或活病毒滴度)。
必須考慮的其它因素以及它們將影響的潛在因素如圖 1 所示。這些包括輸入考慮因素(例如 SUT 和不銹鋼系統之間的選擇)和輸出考慮因素(包括定義關鍵規模縮放參數)。如果在考慮這些因素時沒有花費足夠的時間和精力,項目很快就會變得非常昂貴,因為它會延遲上市時間。
規模縮小模型
適當規模縮小模型的使用和確認至關重要,因為它可以降低成本并縮短時間。實驗設計 (DoE) 和多變量數據分析 (MVDA) 方法的使用可用于實現更高吞吐量的工藝建模。例如,Sartorius Ambr 250 和 Ambr 15 系統分別支持多達 24 或 48 個并行化和微型化生物反應器的上游規模縮小建模。
這種規模縮小的 DoE 工作可以定義關鍵操作/過程/材料參數、關鍵控制參數/設定點和操作/可接受范圍及其對產品關鍵質量屬性的影響。提供額外的支持性、基于風險的規模放大/縮小模擬軟件(Sartorius、BioPat Process Insights)可以顯著減少工作量,從而縮短成功規模放大操作的時間線,并降低后期昂貴失敗的風險。
上游工藝的可放大性
圍繞可放大性的挑戰主要涉及上游生物反應器的放大,因為與下游工藝 (DSP) 步驟的線性放大相比,這通常更為復雜。這種復雜性進一步加劇了與所選宿主細胞系相關的挑戰,因為其關鍵性能指標對于規模放大和縮小至關重要。根據細胞系是否可以作為貼壁或懸浮生長,將極大地影響規模縮放過程中所需的考慮因素。許多一次性生物反應器在設計時都考慮到了可放大性,以緩解貼壁細胞系和懸浮細胞系上游開發中的潛在困難。
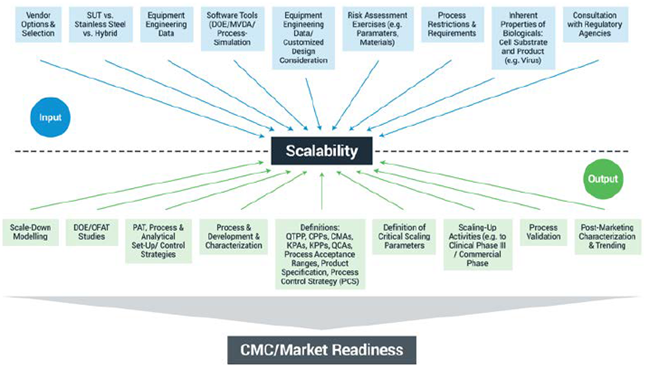
圖 1. 確定工藝可放大性時的輸入注意事項和潛在輸出
放大懸浮細胞上游工藝
放大懸浮培養的早期階段大多是直截了當的。搖瓶的體積范圍為 125 mL 至 5 L,可對所有常用細胞系(例如 CHO-S、HEK293/T、HeLa S3)進行線性規模放大。在規模之間,工作體積通常保持恒定,典型值為 10-30%。當推進到生物反應器規模時,在擴大懸浮細胞培養規模時必須考慮幾個重要參數,其中一些在表 I 中有詳細說明。
當旨在創建無縫規模放大和縮小時,選擇本質上設計為能夠在所有可用規模之間轉移工藝的生物反應器系統至關重要。
供應商通常會將他們的一次性生物反應器開發為圓柱形(盡管也有例外,例如立方體形狀的 PALL),高度和直徑(袋高/直徑)和 d/D(葉輪直徑/袋直徑)的比例恒定)。具有恒定的幾何設計有利于規模放大參數,例如特異性功率輸入、kLa 和混合時間。
放大貼壁細胞上游工藝
貼壁細胞培養的規模放大以前并不容易,并且依賴于可放大的、基于微載體的工藝的擴展和開發。
橫向規模擴展涉及增加培養單元的數量(例如,T瓶、滾瓶、CellSTACK [康寧])。與規模放大技術相比,規模擴展需要大量的操作員操作,并且存在固有的高污染風險。操作挑戰也經常出現,因為某些主要與細胞相關的工藝參數必須仔細考慮和控制。放大基于微載體的工藝也不是一件容易的事,并不適合所有細胞系和產品組合(例如,對某些病毒來說很困難)。
幸運的是,一次性封閉操作和線性可放大的固定床生物反應器系統現已進入市場空間,供應商包括 PALL (iCELLis)、Univercells Technologies (scale-X) 和 Corning (ASCENT)。這些系統的工程設計通常旨在實現無縫規模放大,同時考慮剪切應力、功率輸入、單位生長表面積的培養基體積以及供氧能力等因素。
所有三種生物反應器都提供用于概念驗證、工藝建立和表征的的規模縮小開發和建模系統。最大的GMP生產規模包括 500 m2 (PALL)、600 m2 (Univercells Technologies) 和 1,000 m2 (Corning)。
DSP 步驟的可放大性
大多數典型的下游工藝允許線性規模放大/縮小。DSP 中的許多工藝都依賴于一次性組件,包括過濾器和層析填料。生產商在使用這些一次性技術時必須意識到 DSP 步驟規模放大中的挑戰,包括識別供應商提供各種規模的技術的能力(特別是對于規模縮小模型)。還必須考慮確定某些一次性技術產品是更適合橫向規模擴展還是縱向規模放大。
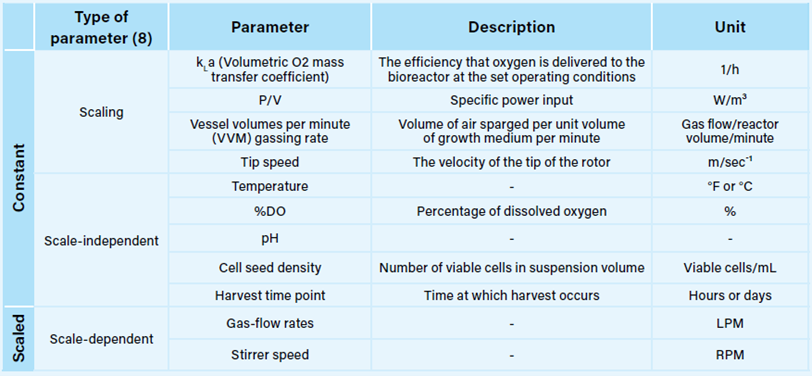
表 I. 懸浮細胞培養規模放大時必須考慮的關鍵常數和縮放參數
直流過濾
直流過濾 (NFF) 操作通常在 DSP 中用于在收獲時進行澄清或在工藝流程的最后階段用于減少生物負荷和終端除菌過濾目的。此類過濾器提供單一孔徑截留膜,或一系列具有從大到小“漏斗”功能的截留膜,以提高過濾能力。
NFF 可以在恒定壓力或恒定通量 [LMH;升/平方米/小時]條件下進行,且產品的潛在剪切應力必須始終考慮在內。規模縮放時,供應商、膜材質和孔徑應保持不變。
膜面積和處理體積應與工藝進料體積成線性比例,由此污染物在不同工藝運行和生產規模之間被視為具有可比性。還應考慮可堆疊(即可并聯)過濾元件,因為它可以在可用膜面積上提供更大的靈活性,覆蓋比獨立囊式濾器更大的規模。
錯流/切向流過濾。
在錯流/切向流過濾 (CFF/TFF) 中,進料以水平液流的形式流過膜;因此,通常可以降低濾膜污染的傾向。關鍵優化參數是通量 (LMH),其與 TMP (bar) 相關。常用的形式是中空纖維組件或平板膜包。
截留分子量 (MWCO) 是一個重要參數,應仔細考慮要去除的污染物的分子量和產品粒徑本身。所有規模條件下的 MWCO 必須保持恒定。
CFF 使用恒定的跨膜壓力或濾液通量 FLUX 進行控制。在規模放大過程中,過濾器負載(單位面積的處理體積)保持穩定。切向流速通常通過保持剪切率恒定而按比例增加。這對于剪切敏感產品(例如,囊膜病毒)是有意義的。
層析。大多數生物生產過程包括至少一個結合/漂洗/洗脫或流穿方式的層析步驟,以富集產品并去除與工藝相關的殘留物。
最常用的模式是親和、離子交換、尺寸排阻、疏水相互作用和復合模式填料。規模放大時,關鍵的線性縮放參數是流速 (cm/h) 或產品保留時間。為保持不同規模的流速恒定,應通過保持柱高恒定并增加柱直徑,使柱體積與要上樣的體積成線性比例增加。
所有緩沖液的體積也應線性縮放,通量率保持恒定(柱體積/小時)。層析柱體積的線性放大并不總是能簡單實現,因為層析柱、膜吸附或整體柱只以特定尺寸提供。
緩解這一問題的選項可以是運行多個產品循環或并行化處理。按恒定柱體積/小時進行放大被用作替代方法,并可能成為某些模式(例如親和、離子交換)的行業標準,有助于避免運行過程超出柱處理量。
規模擴展 vs. 規模放大
改變現有設施的規模,例如天花板高度、高壓滅菌柜容量、地板重量負載、氣體供應能力、液體處理單元和種子擴增鏈的變化可能會帶來重大挑戰。因此,規模擴展通常被視為比向上規模放大更可行的替代方案,可提供生產靈活性并更好地適應市場波動。SUT 特別適合這種策略。
工藝驗證也更直接;通過使用框架驗證設計,不需要額外的驗證。橫向規模擴展生產還意味著,如果發生故障(取決于根本原因),整批產品不會丟失,而只會丟失一個單元。隨著現在有更多選項可用于成功的工藝強化,橫向規模擴展已成為對 ATMP 生產商越來越有吸引力的選擇。
關鍵知識
在放大 ATMP 生產工藝時,必須考慮許多重要的因素,以提供靈活性和可放大性。SUT 非常適合 ATMP 生產,尤其是在橫向規模擴展時。隨著 SUT 的進步及其不同尺寸的可用性,這些技術的采用可能會變得越來越流行。然而,生產商在使用 SUT 進行規模擴展時仍將面臨挑戰,并且需要了解和考慮可能會在不斷變化的規模上受到影響的所有工藝參數。
原文:K.Lipinski, Scaling Manufacturing Processes Using Single-Use Technologies. Pharmaceutical technology, 2023.






